Дермальные адипоциты в дерматологии и эстетической медицине: факты и гипотезы
ВВЕДЕНИЕ
Современные методы лечения в дерматологии и эстетической медицине базируются на известных анатомических и физиологических особенностях кожи. Эти особенности лежат в основе тех или иных теоретических моделей кожи, которые должны учитывать ее механические свойства, характерные времена турновера (turnover), миграцию клеток и др. Один из основных принципов дерматологии предполагает, что фенотипические признаки клеток кожи изменяются с течением времени несущественно, т.е. что клетки терминально дифференцированы. Следовательно, фибробласт всегда должен оставаться фибробластом и производить коллаген и другие компоненты внеклеточного матрикса, чтобы гарантировать стабильность структуры кожи.
Однако если вдруг окажется, что эпителиальные клетки могут превращаться в мезенхимальные и, наоборот, что миофибробласты в действительности не являются терминально дифференцированными клетками, а могут соответствующим образом себя ре- или дедифференцировать и что адипоциты (которые теоретически даже не должны были бы быть расположены в коже) позволяют себя трансдифференцировать в миофибробласты, «безмятежный» до сих пор мир дерматологии, по-видимому, может дрогнуть. И тогда рано или поздно придется провести ревизию основополагающих теорий.
Похоже, что именно такая «ревизия» как раз и происходит сегодня. Виновники этого – так называемые «дермальные адипоциты». Теоретически дермальные адипоциты должны представлять собой, скорее, исключение и не играть в дерме никакой важной физиологической роли. Об этом свидетельствуют совсем небольшое количество этих клеток в коже (по сравнению с такими «глобальными игроками», как фибробласты и кератиноциты), а также большой объем, занимаемый сетью коллагена и другими специальными внеклеточными структурами, которые не должны быть физиологически связаны с функционированием адипоцитов. Уже из одного этого факта должно вытекать, что такие процессы как, например, заживление ран, образование рубцов или старение кожи, могут в лучшем случае лишь косвенно быть связаны с адипоцитами.
КОЖНЫЕ АДИПОЦИТЫ – АУТСАЙДЕРЫ ИЛИ МЕГАГЛОБАЛЬНЫЕ ИГРОКИ?
Давно известно, что 2 разных анатомических слоя жировой ткани находятся под ретикулярной дермой. У грызунов эти слои разделены поперечно- полосатой мышцей (так называемой m. panniculus carnosus) и оттого отчетливо заметны. В человеческой коже также есть дермальные адипоциты, однако они концентрируются преимущественно вокруг волосяных фолликулов.
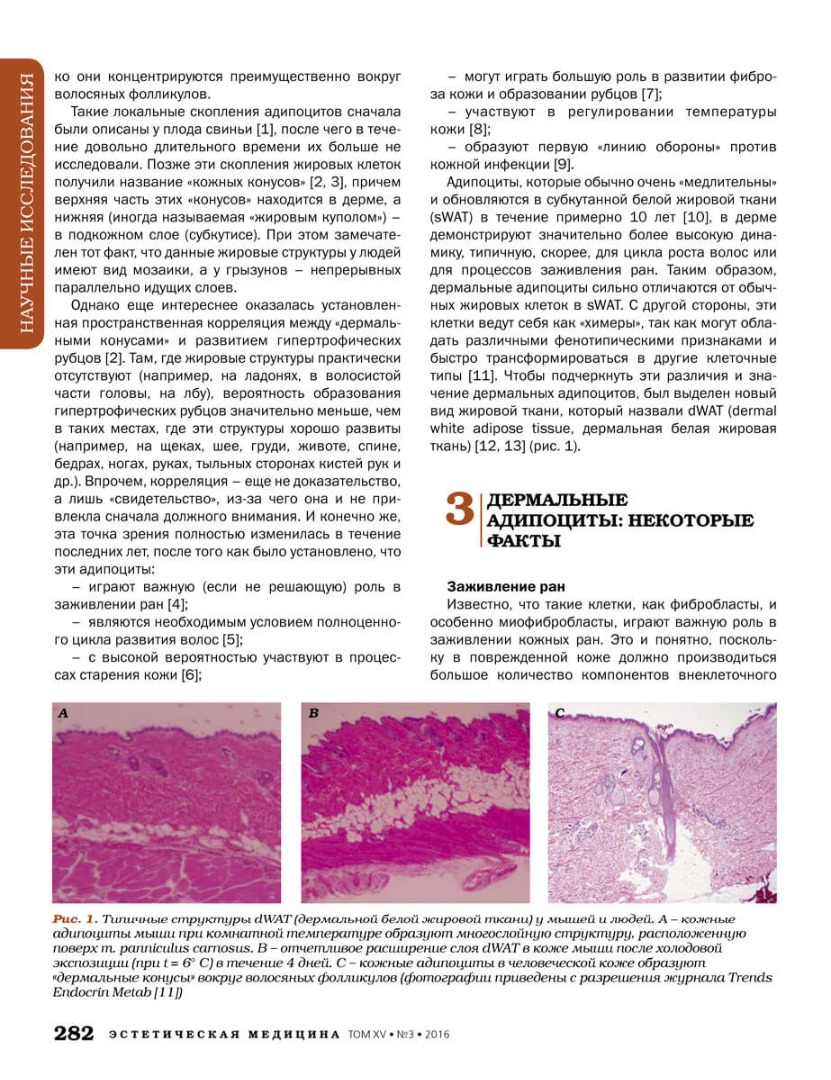
Такие локальные скопления адипоцитов сначала были описаны у плода свиньи [1], после чего в течение довольно длительного времени их больше не исследовали. Позже эти скопления жировых клеток получили название «кожных конусов» [2, 3], причем верхняя часть этих «конусов» находится в дерме, а нижняя (иногда называемая «жировым куполом») – в подкожном слое (субкутисе). При этом замечателен тот факт, что данные жировые структуры у людей имеют вид мозаики, а у грызунов – непрерывных параллельно идущих слоев.
Однако еще интереснее оказалась установленная пространственная корреляция между «дермальными конусами» и развитием гипертрофических рубцов [2]. Там, где жировые структуры практически отсутствуют (например, на ладонях, в волосистой части головы, на лбу), вероятность образования гипертрофических рубцов значительно меньше, чем в таких местах, где эти структуры хорошо развиты (например, на щеках, шее, груди, животе, спине, бедрах, ногах, руках, тыльных сторонах кистей рук и др.). Впрочем, корреляция – еще не доказательство, а лишь «свидетельство», из-за чего она и не привлекла сначала должного внимания. И конечно же, эта точка зрения полностью изменилась в течение последних лет, после того как было установлено, что эти адипоциты:
– играют важную (если не решающую) роль в заживлении ран [4];
– являются необходимым условием полноценно- го цикла развития волос [5];
– с высокой вероятностью участвуют в процес- сах старения кожи [6];
– могут играть большую роль в развитии фибро- за кожи и образовании рубцов [7];
– участвуют в регулировании температуры кожи [8];
– образуют первую «линию обороны» против кожной инфекции [9].
Адипоциты, которые обычно очень «медлительны» и обновляются в субкутанной белой жировой ткани (sWAT) в течение примерно 10 лет [10], в дерме демонстрируют значительно более высокую динамику, типичную, скорее, для цикла роста волос или для процессов заживления ран. Таким образом, дермальные адипоциты сильно отличаются от обычных жировых клеток в sWAT. С другой стороны, эти клетки ведут себя как «химеры», так как могут обладать различными фенотипическими признаками и быстро трансформироваться в другие клеточные типы [11]. Чтобы подчеркнуть эти различия и значение дермальных адипоцитов, был выделен новый вид жировой ткани, который назвали dWAT (dermal white adipose tissue, дермальная белая жировая ткань) [12, 13]
ДЕРМАЛЬНЫЕ АДИПОЦИТЫ: НЕКОТОРЫЕ ФАКТЫ
Заживление ран
Известно, что такие клетки, как фибробласты, и особенно миофибробласты, играют важную роль в заживлении кожных ран. Это и понятно, поскольку в поврежденной коже должно производиться большое количество компонентов внеклеточного матрикса. Однако то, что кожные адипоциты засе- ляют рану параллельно с фибробластами и что этот процесс реализуется посредством адипогенеза, – относительно новые данные [4]. Было показано, что мыши с генетически обусловленной липоатрофией (т.н. мыши А ZIP/F1), у которых зрелые адипоциты отсутствуют на системном уровне, демонстрируют образование у них дефектных фибробластов и нестабильное заживление кожных ран, что подчеркивает значение зрелых дермальных адипоцитов в этом процессе.
Вместе с тем у этого положительного свойства дермальных адипоцитов есть и оборотная сторона: раз уж они вовлечены в заживление кожных ран, они должны играть не менее важную роль и в образовании рубцов.
Образование рубцов
До сих пор образование фиброза в ходе заживления кожных ран связывали преимущественно с недостаточным апоптозом миофибробластов. Эти клетки должны «умирать» в поздних фазах заживления, чтобы избежать перепроизводства коллагена в ране. Считалось, что миофибробласты могут образовываться из имеющихся фибробластов или клеток эпителия путем так называемого эпителиально-мезенхимального трансдифференцирования. Такая трансформация должна быть обратима, поскольку адипоциты могут редифференцироваться в эпителиальные клетки [14]. Для образования рубцов нужны малоподвижные коллагенобразующие миофибробласты с высокой синтетической активностью. Могут ли эти миофибробласты производиться из адипоцитов?
Через 2 года после работы Schmidt и Horsley [4] появилась важная публикация [7], которая ответила на этот вопрос положительно. В ней было продемонстрировано, что развитие дермального фиброза хорошо коррелирует с потерей dWAT. Это значит, что жировая ткань замещается фиброзными тяжами.
Было также показано, что миофибробласты производятся из адипонектин-положительных стволовых клеток. Этот эффект назвали «адипоцит-миофибробластной трансформацией», и сегодня представляется, что этот новый вид клеточной дифференцировки может играть значительно бόльшую роль в различных физиологических и патологических процессах, чем это думали первоначально [11]. Отсюда следует парадокс: с одной стороны, дермальные адипоциты необ- ходимы для полноценного заживления кожных ран, с другой – они значительно повышают риск образования гипертрофических рубцов из-за их потенциальной дифференцировки в миофибробласты.
Цикл роста волос
Едва ли кто-либо в настоящее время сомневается в том, что дермальные адипоциты активно участвуют в цикле роста волос [5]. Присутствие этих клеток представляется не только необходимым, но и достаточным для нормального циклического развития волосяных фолликулов. В этой связи интересно, что в плодах мышей dWAT развивается независимо от sWAT и что это развитие в основном связано с морфогенезом волосяных фолликулов. [12]. Это значит, что дермальные адипоциты (dWAT) должны значительно отличаться от адипоцитов подкожного белого жира (sWAT).
Зрелые адипоциты и адипозные стволовые клет- ки по-разному представлены в различных фазах цикла роста волос. В начале фазы анагена количество преадипоцитов в коже мышей 4-кратно увеличивается, но возвращается к норме в конце этой фазы. Зрелые адипоциты присутствуют преимущественно во время развития стержня волоса в VI под- фазе анагена, однако их количество в фазах катагена и телогена отчетливо сокращено. Это частично объясняет, почему волосяные мешочки в VI подфазе анагена гораздо менее чувствительны к свету, чем в других его подфазах [15–18].
Существующая корреляция между фазами роста волос и количеством dWAT ведет к изменению вида и состояния кожи. Так как в тех местах, где волосы находятся в фазе анагена, количество dWAT должно был больше, чем в других, можно предположить, что должно возникать пространственно гетерогенное распределение жировой ткани [19]. Это может вести к образованию пространственно ограниченных областей кожи, на границе которых могут возникать градиенты производимых адипоцитами паракринных сигналов. А это, в свою очередь, говорит о том, что структура кожи и соответственно ее функции должны быть гетерогенны – аспект который ни в дерматологии, ни в эстетической медицине до сих пор не учитывался.
Гомеостатическая терморегуляция
В последнее время обнаружился очередной сюрприз: dWAT должна быть вовлечена в гомеостатическую терморегуляцию. Это показали эксперименты на мышах, у которых не вырабатывается белок Syndecan-1 [8]. Syndecan-1 необходим для полноценной дифференцировки адипоцитов, без этого белка dWAT-слой остается сильно недоразвит. На этой модели было показано, что кожа может реагировать на изменение условий окружающей среды быстрой инволюцией или экспансией dWAT-слоя. В то время как sWAT обычно реагирует на «мягкий» холод высвобождением глицерина и выработкой бурых/«бежевых»адипоцитов, dWAT-слой при тех же самых температурах быстро увеличивается в толщину до 4 раз (см. рис. 1 В). Эта жировая экспансия обратима – после возвращения к нормальным температурам толщина dWAT-слоя быстро сокращается и возвращается к своим нормальным значениям. Неодинаковая реакция dWAT и sWAT на изменение температуры окружающей среды также указывает на разные свойства адипоцитов этих 2 видов жировой ткани.
Иммунная защита кожи
Уже давно предполагалось, что адипоциты могут обладать иммунной активностью. Совсем недавно это было наконец доказано [9]. После того, как кожу мышей инфицировали золотистым стафилококком (S. аureus), жировая ткань отреагировала на заражение быстрым увеличением количества преадипоцитов и многократным увеличением толщины dWAT- слоя. Было отмечено, что, по крайней мере, частично это вызвано гипертрофией уже существующих адипоцитов. Оказалось, что у мышей с подавленной экспансией dWAT-слоя иммунный ответ на S. aureus понижен. Описанная иммунная реакция была обусловлена выработкой адипоцитами антимикробного пептида кателицидина (Cathelicidine). Это может свидетельствовать о существовании неожиданной связи между дермальными адипоцитами и воспалительны- ми кожными заболеваниями, так как кателицидины могут стимулировать воспалительную реакцию.
4 ДЕРМАЛЬНЫЕ АДИПОЦИТЫ: НЕКОТОРЫЕ ГИПОТЕЗЫ
Воспалительные кожные заболевания (эффлоресценции)
Сегодня мы можем предположить, что дермальные адипоциты вовлечены в развитие различных воспалительных кожных заболеваний [11, 20]. Это подтверждается тем фактом, что концентрация производимого ими антимикробного пептида кателицидина, обладающего провоспалительным действием, значительно повышена в коже, пораженной розацеа и псориазом [21]. Производство кателицидина существенно меняется и при атопическом дерматите [22]. Известно также, что антимикробные пептиды активно участвуют в патофизиологии угревой сыпи [23], недавно кателицидин был даже предложен в качестве возможного варианта лечения акне [24].
Поскольку dWAT участвует в патофизиологии различных воспалительных кожных заболеваний, можно предположить, что толщина dWAT-слоя должна быть локально увеличена в тех участках кожи, которые поражены розацеа и псориазом. Такое поведение жировой ткани не является необычным, если учиты- вать, что воспаление может сильно стимулировать местный адипогенез, поскольку это необходимо для здорового ремоделирования жировой ткани [25].
Модуляция толщины dWAT-слоя уже была продемонстрирована на различных генно-модифицированных нокаутных моделях [11]. Недавно было также пока- зано, что адипонектин (известный как метаболический регулятор чувствительности к инсулину) участвует в развитии псориазоподобного дерматита у мышей [26]. Более того, мыши, у которых выработка адипонектина генетически блокирована, демонстрируют тяжелую форму этого заболевания, что опять-таки указывает на связь между псориазом и адипоцитами. Дальнейшие исследования должны показать, в какой мере dWAT-структуры фактически участвуют в патогенезе различных воспалительных поражений кожи.
Известно, что большинство воспалительных кожных заболеваний реагируют на воздействие одних и тех же физических факторов улучшением состояния кожи. Такая неспецифическая реакция была продемонстрирована после воздействия высокочастотным ультразвуком (с частотой 10 МГц) на пораженную кожу при таких заболеваниях, как розацеа, экзема, акне и псориаз [27]. Это говорит о том, что все перечисленные заболевания должны иметь как минимум один общий неспецифический патофизиологический компонент. Такое неспецифическое воздействие высокочастотного ультразвука было обосновано локальным регулированием выработки матричных металлопротеиназ [27]. Даже если содержание матричных металлопротеиназ может быть фактически повышено в воспаленной коже на несколько порядков, такое увеличение – не первопричина, а, скорее, следствие кожной эффлоресценции. В то же время нарушение выработки кателицидина дермальными адипоцитами может претендовать на роль патофизиологического компонента в развитии воспалительных кожных заболеваний.
Старение кожи
Процессы старения характеризуются уменьшением объема жировых отложений и увеличением локального фиброзирования ткани. Инволюция жировой ткани может быть реализована путем уменьшения размеров отдельных адипоцитов, их гибели или путем дифференцировки адипоцитов в другие клетки (например, в фибробласты). Описанные выше процессы дифференцировки, при которых адипоциты превращаются в клетки эпителия или миофибробласты, вызывают локальное уменьшение объема жировой ткани. Локальные потери жира в «дермальных конусах» (в пределах некоторой характерной площади) приводят к неоднородному изменению структуры кожи. Так как процессы деградации в папиллярном слое дермы и в dWAT-слое могут идти параллельно и независимо друг от друга, следует предположить, что старение кожи может осуществляться в различных формах.
В пользу этого имеются несколько сильных аргументов. Долговременное УФ-облучение безволосых мышей не приводит к уплотнению их дермы, но вызывает значительное сокращение толщины dWAT-слоя, что сопровождается развитием фиброза и накоплением гиалуроновой кислоты [28]. В другом эксперименте мышей подвергали долговременному УФA-облучению [29]. В этом случае также наблюдали отчетливое сокращение dWAT-слоя (правда, только через 8 недель облучения) и развитие фиброза. Так как в обоих экспериментах никакого уплотнения дермы не наблюдали, можно предположить (по крайней мере, в отношении фотоиндуцированного старения кожи), что описанные выше процессы трансформации адипоцитов в миофибробласты играют важную патофизиологическую роль. Это должно означать, что УФ-облучение может инициировать трансдифференцировку дермальных адипоцитов и преобразование их в синтетически активные миофибробласты. Если это предположение верно, то основную гипотезу старения кожи можно ставить под сомнение и переместить главное внимание анти-эйдж-терапии с соединительной ткани (т.е. дермы) на поверхностный слой субкутиса (т.е. на подкожно-жировую клетчатку).
Эффективная коррекция стареющей кожи должна также затрагивать и процессы, происходящие в жировой ткани. Недавно было высказано мнение, что широко распространенные сегодня наполнители мягких тканей (филеры), прежде всего, должны влиять не на производство коллагена, а на адипогенез [31]. Это могло бы объяснять не только моментальное, но и долгосрочное улучшение состояния кожи после введения филеров, однако требует принципиального пересмотра последовательности используемых для коррекции процедур. Можно предположить, что филер не следует применять сам по себе – для получения хорошего результата прежде, чем его вводить, надо было бы выполнить специальную обработку реципиентной зоны.
Гипер- и гипопигментации кожи
Патофизиология мелазмы базируется на локальном повышении активности меланоцитов, которое традиционно объясняется воздействием УФ-облучения [32]. Однако на меланоциты можно воздействовать не только непосредственно ультрафиолетовым светом, но и с помощью паракринных сигналов. Эти сигналы переносятся посредством диффузии, что сильно ограничивает радиус их действия. Чтобы эффективно воздействовать на меланоциты, сигналпродуцирующие клетки не должны быть значительно удалены от эпидермиса.
Важное невыясненное свойство гиперпигментации – ее мозаичный характер: размеры пигментных пятен обычно значительно больше, чем размеры самих меланоцитов. Таким образом, формирование гиперпигментации в виде макулы (ограниченного по размерам участка пораженной кожи) требует согласованной реакции меланоцитов на этом участке. Ограниченный размер макул пытались связать с деятельностью эпителиальных клеток [33]. Но в последнее время предположили, что в развитии гипер- и гипопигментации кожи важную роль могут играть дермальные адипоциты [11].
Известно, что стволовые клетки жировой ткани могут подавлять производство меланина как in vitro [34], так и in vivo (при внутрикожных инъекциях) [35], что можно объяснить увеличением секреции фактора роста TGF-β1. Это известный медиатор паракринных сигналов, который также определяет профили экспрессии в коже гиалуроновой кислоты и различных видов коллагена [36]. Одновременно TGF-β1 подавляет продукцию тирозиназы, что должно привести к ингибированию синтеза меланина.
Это значит, что dWAT в принципе может быть вовлечена в регуляцию продукции меланина. Так как размер пятен мелазмы или поствоспалительной гиперпигментации намного превосходит и размеры отдельных меланоцитов, и размеры отдельных dWAT-структур, возникает вопрос, не связана ли гиперпигментация с уменьшением секреции TGF-β1 в dWAT-структурах характерных участков кожи [19]?
5 ВОЗМОЖНЫЕ ИЗМЕНЕНИЯ В ЛЕЧЕБНЫХ И КОРРЕКТИРУЮЩИХ ПРОЦЕДУРАХ В ДЕРМАТОЛОГИИ И ЭСТЕТИЧЕСКОЙ МЕДИЦИНЕ
Поскольку особые свойства дермальных адипоцитов нельзя дальше игнорировать, можно предположить, что в будущем в некоторых дерматологическихи эстетических процедурных программах и концепциях лечения произойдут важные изменения. Физические факторы, которые могут модифицировать стволовые клетки и зрелые адипоциты, ведут себя в некоторых случаях так же, как факторы, которые применяют для стимуляции неоколлагеногенеза. С другой стороны, между ними имеются и большие отличия. Например, стимуляцию работы адипоцитов можно вызвать, оказывая на ткани механическое воздействие, путем «мягкого» нагревания или охлаждения, причем сила этой стимуляции будет зависеть от параметров воздействия. В то же время холодовые процедуры не ведут к стимуляции коллагеногенеза – здесь отчетливо видны различия.
Особенность стимуляции дермальных адипоцитов в том, что они находятся на границе дермы и подкожной клетчатки. Следовательно, стимуляция этих клеток требует концентрации воздействия именно в этом слое, что само по себе нелегкая задача, особенно если учитывать значительные колебания толщины дермы в пределах обрабатываемой зоны, а также у разных пациентов. Вероятно, в эстетической медицине речь впервые идет о смене объекта воздействия корректирующих процедур – с объема ткани на пограничный слой «дерма/подкожно-жировая клетчатка».
Подобное изменение парадигмы может привести к тому, что многие дерматологические и эстетические задачи невозможно будет удовлетворительно решать «автономными» методами и придется перейти преимущественно к комбинированной коррекции. К тому же стимуляция дермальных адипоцитов, вероятно, потребует значительного увеличения частоты процедур и потому не сможет быть оптимально реализована амбулаторно. Соответственно в будущем пациентов придется более активно вовлекать в процесс лечения.
6 ЗАКЛЮЧЕНИЕ
Дермальные адипоциты – специфические клетки, которые участвуют в различных физиологических и патологических процессах в коже. Эти клетки могут быстро развиться из стволовых клеток жировой ткани, с другой стороны, они могут превращаться в эпителиальные клетки или фибробласты, что говорит об их большой пластичности. Дермальные адипоциты демонстрируют динамику развития, которая может в 1000 раз превышать показатели, свойственные субкутанным адипоцитам. Реакция dWAT на воздействие различных экзогенных факторов может привести к значительному увеличению или уменьшению толщины дермальных жировых структур, а это должно иметь последствия для решения не только дерматологических, но и эстетических проблем.
Можно исходить из того, что новые концепции и методы лечения в дерматологии и эстетической медицине будут не только учитывать возможность воздействия на дермальные адипоциты, но и базироваться на таком воздействии. Поскольку оптимальное воздействие на коллагеновые структуры и дермальные адипоциты, скорее всего, может быть достигнуто только в результате применения разных физических факторов и различных параметров лечения, следует предположить, что многие дерматологические и эстетические проблемы не будут удовлетворительно решены с помощью какого-либо одного метода или одной процедуры, а потребуют комбинации нескольких методов и/ или процедур.
ЛИТЕРАТУРА
1. Hausman GJ, Martin RJ. The development of adipocytes located around hair follicles in the fetal pig. J Animal Sci, 1982;54:1286–1296.
2. Matsumura H, Engrav LH, Gibran NS, et al. Cones of skin occur where hypertrophic scar occurs. Wound Repair Regen, 2001;9:269–277.
3. Engrav LH, Tuggle CK, Kerr KF, et al. Functional genomics unique to week 20 post wounding in the deep cone/fat dome of the Duroc/Yorkshire porcine model of fibroproliferative scarring. PloS ONE, 2011;6:e19024.25.
4. Schmidt BA, Horsley V. Intradermal adipocytes mediate fibroblast recruitment during skin wound healing. Develop, 2013;140:1517–1527.
5. Festa E, Fretz J, Berry R, et al. Adipocyte lineage cells contribute to the skin stem cell niche to drive hair cycling. Cell, 2011;146:761–771.
6. Rivera-Gonzalez G, Shook B, Horsley V. Adipocytes in Skin Health and Disease. Cold Spring Harbor Pers Medicine, 2014;4:a015271.
7. Marangoni RG, Korman BD, Wei J, et al. Miofibroblasts in cutaneous fibrosis originate from adiponectinpositive intradermal progenitors. Arthrit Rheumatol, 2015;67:1062–1073.
8. Kasza I, Suh Y, Wollny D, et al. Syndecan-1 is required to maintain intradermal fat and prevent cold stress. PLoS Genet, 2014;10:e1004514.
9. Zhang LJ, Guerrero-Juarez CF, Hata T, et al. Dermal adipocytes protect against invasive Staphylococcus aureus skin infection. Science, 2015;347:67–71.
10. Spalding KL, Arner E, Westermark PO, et al. Dynamics of fat cell turnover in humans. Nature, 2008;453:783–787.
11. Kruglikov IL, Scherer PE. Dermal adipocytes: from irrelevance to metabolic targets? Trends Endocrin Metabol, 2015;27:1–10.
12. Wojciechowicz K, Gledhill K, Ambler CA, et al. Development of the mouse dermal adipose layer occurs independently of subcutaneous adipose tissue and is marked by restricted early expression of FABP4. PloS ONE, 2013;8:e59811.
13. Driskell RR, Jahoda CAB, Chuong CM, et al. Defining dermal adipose tissue. Exp Dermatol, 2014;23:629–631.
14. Morroni M, Giordano A, Zingaretti MC, et al. Reversible transdifferentiation of secretory epithelial cells into adipocytes in the mammary gland. Proc Nat Acad Sci, 2004;101:16801–16806.
15. Kruglikov IL. Melanin light absorption as the necessary but not sufficient condition for photoepilation: Intraanagen variability of hair follicle light sensitivity. Am J Cosm Surg, 2012a:29:266–272.
16. Kruglikov IL. Kontroversen in der sthetischen Medizin: 2. Simplex sigillum veri der Photoepilation. Kosmet Med, 2012b:33:238–242.
17. Kruglikov IL. Melanin light absorption as the necessary but not sufficient condition for photoepilation: miniaturization and eclipse phenomena. Am J Cosmet Surg, 2013;30:21–27.
18. Kruglikov IL. Possible role of dermal adipocytes in intraanagen variation of hair follicle light sensitivity. Am J Cosmet Surg, 2016;33. To be published.
19. Kruglikov IL, Scherer PE. Dermal adipocytes and hair cycling: Is spatial heterogeneity a characteristic feature of the dermal adipose tissue depot? Exper Dermatol, 2016;25:258–262.
20. Kruglikov IL, Scherer PE, Wollina U. Are dermal adipocytes involved in psoriasis? Exp Dermatol, 2016; doi: 10.1111/exd.12996.
21. Yamasaki K, Di Nardo A, Bardan A, et al. Increased serine protease activity and cathelicidin promotes skin inflammation in rosacea. Nature Med, 2007;13:975–980.
22. Reinholz M, Ruzicka T, Schauber J. Cathelicidin LL-37: an anti-microbial peptide with a role in inflammatory skin disease. Ann Dermatol, 2012;126–135.
23. Harder J, Tsuruta D, Murakami M, Kurokawa I. What is the role of antimicrobial peptides (AMP) in acne vulgaris? Exp Dermatol, 2013;22:386–391.
24. Wang Y, Zhang Z, Chen L, et al. Cathelicidin-BF, a snake cathelicidin-derived antimicrobial peptide, could be an excellent therapeutic agent for acne vulgaris. PLoS ONE, 2011;6:e22120.
25. Asterholm IW, Tao C, Morley TS, et al. Adipocyte inflammation is essential for healthy adipose tissue expansion and remodeling. Cell Metabol, 2014;20:103– 118.
26. Shibata S, Tada Y, Hau CS, et al. Adiponectin regulates psoriasiform skin inflammation by suppressing IL-17 production from γδ-T cells. J Immunol, 2012:6:7687.
27. Kruglikov IL. Sehr hochfrequenter Ultraschall als neues Therapieverfahren in der Ästhetik und Dermatologie. Hautarzt, 2015b;66:829–833.
28. Mitani H, Koshiishi I, Toyoda H, et al. Alterations of hairless mouse skin exposed to chronic UV irradiation and its prevention by hydrocortisone. Photochem Photobiol, 1999;69:41–46.
29. Sayama A, Soushin T, Okada T, et al. Morphological and biochemical changes during aging and photoaging of the skin of C57BL/6J mice. J Toxicol Pathol, 2010;23:133– 139.
30. Wollina U. Midfacial rejuvenation by hyaluronic acid fillers and subcutaneous adipose tissue – A new concept. Med Hypoth, 2015;84:327–330.
31. Kruglikov IL, Wollina U. Soft tissue fillers as non-specific modulators of adipogenesis: change of paradigm? Exp Dermatol, 2015a;24:912–915.
32. Goorochurn R, Viennet C, Granger C, et al. Biological processes in solar lentigo: insights brought by experimental models. Exp Dermatol, 2016; doi: 10.1111/ exd.12937.
33. Weiner L, Fu W, Chirico WJ, Brissette JL. Skin as a living coloring book: how epithelial cells create patterns of pigmentation. Pigment Cell Melanoma Res, 2014;27:1014–1031.
34. Kim WS, Park SH, Ahn SJ, et al. Whitening effect of adipose-derived stem cells: A critical role of TGF-beta1. Biol Pharm Bull, 2008;31:606–610.
35. Chang H, Park JH, Min KH, et al. Whitening effects of adipose-derived stem cells: a preliminary in vivo study. Aesth Plast Surg, 2014;38:230–233.
36. Jung H, Kim HH, Lee DH, et al. Transforming growth factor-beta 1 in adipose derived stem cells conditioned medium is a dominant paracrine mediator determines hyaluronic acid and collagen expression profile. Cytotech, 2011;63:57–66.